Publié le 30.07.2025
Le syndrome des plaquettes grises (SPG) est une maladie très rare (environ 60 cas ont été décrit à l’heure actuelle), qui affecte autant les hommes que les femmes. Les premiers symptômes apparaissent généralement dans la période néonatale ou la petite enfance : faible nombre de plaquettes, saignements, plaquettes anormales…
Il n'existe actuellement pas de traitement spécifique pour le SPG, seulement des mesures de prévention du risque hémorragique (par exemple, la transfusion de plaquettes avant une intervention chirurgicale).
Le SPG est dû à des mutations sur le gène NBEAL2. En l’absence de NBEAL2, les plaquettes ne possèdent presque plus de protéines essentielles à l’arrêt d’un saignement. Par ailleurs, il a été observé que certains patients développent dans un second temps une maladie auto-immune, ce qui suggère un lien encore inconnu de NBEAL2 avec la réponse immunitaire.
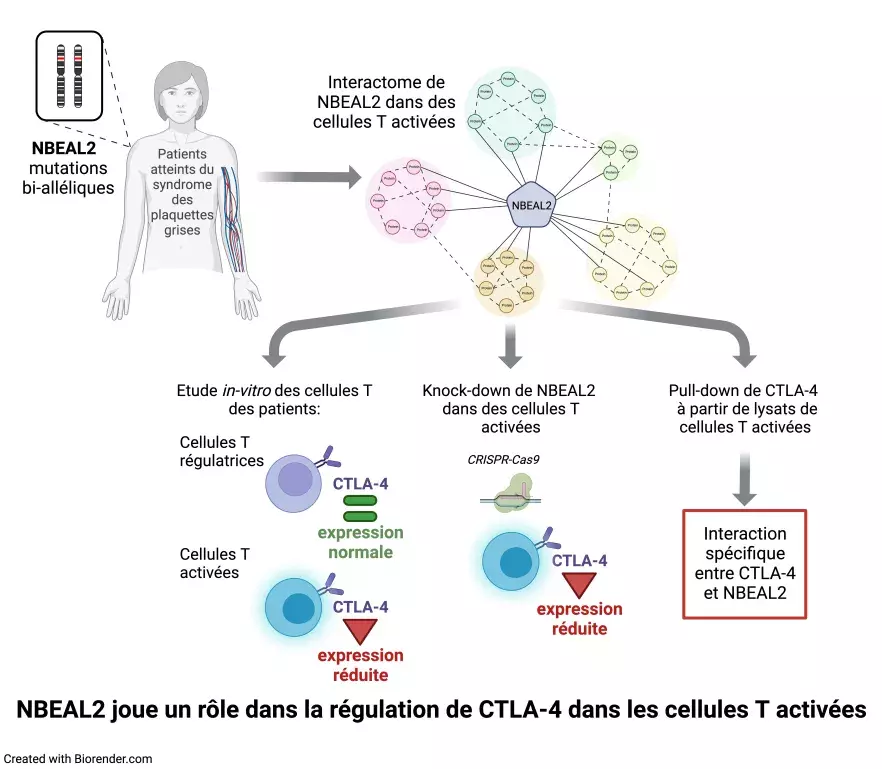
A travers ce prisme, en collaboration avec Sanofi, le laboratoire « Immunogénétique des maladies auto-immunes pédiatriques » dirigé par Frédéric Rieux-Laucat à l’Institut Imagine (Inserm, AP-HP, Université Paris Cité) a identifié les partenaires intracellulaires de NBEAL2. Pour ce faire, Laure Delage a établi un « interactome » de NBEAL2 (une liste exhaustive des protéines avec lesquelles NBEAL2 semble interagir) dans les lymphocytes T. Parmi ces partenaires potentiels, les chercheurs ont remarqué la protéine CTLA-4, par ailleurs impliquée dans la réponse immunitaire et l’apparition de maladies auto-immunes. Ils ont ensuite confirmé de manière spécifique que CTLA-4 et NBEAL2 interagissent l’un avec l’autre dans les cellules immunitaires : c’est bien l’absence de NBEAL2 qui va réduire le niveau, et donc l’activité, de CTLA-4.
Les résultats de cette étude montrent que NBEAL2 joue bien un rôle spécifique dans la réponse immunitaire, en régulant l’activité de CTLA-4, acteur-clé de l’apparition de maladies auto-immunes. Ces travaux ouvrent donc de nouvelles options thérapeutiques pour les patients atteints de SPG qui souffrent de maladies auto-immunes, puisqu’une thérapie ciblée utilisant du CTLA-4 exogène permettrait de compenser le défaut d’expression de CTLA-4 sur les lymphocytes des patients SPG.